引言
2022年1季度NMPA共批准了12款新药,其中3个国产1类新药,其余9款为进口药物在国内首次获批。从适应症上来看,有3个用于肿瘤的治疗,2个新冠药物,1个罕见病药物。
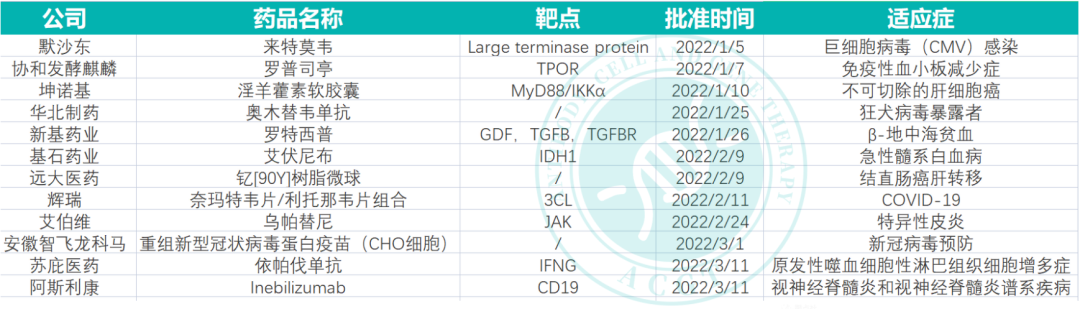
2022年第一季度NMPA批准的12款药物
淫羊藿素软胶囊
淫羊藿素软胶囊是2022年首个获批上市的1类创新药,也是少见的中药创新药。淫羊藿素化学全称为异戊烯类黄酮化合物(3,5,7-三羟基-2-(4-甲氧基苯基)-8-(3-甲基丁-2-烯基)-4H-苯并吡喃-4-酮),属于小分子免疫调节类抗肿瘤药物,通过直接结合MyD88/IKKα,抑制TLR-MyD88-IKK-NF-κB炎症通路,从而减少TNF-α、IL-6等炎症因子产生,下调IL6-JAK2-STAT3通路。分子通过直接结合IKKα,也抑制TNF-α对IKK-NF-κB信号通路的活化,进而抑制PD-L1表达和降低抑制型免疫细胞MDSC,活化IFN-γ阳性CD8+T细胞,发挥免疫调节及抗肿瘤作用。
这是首个针对IKKα靶点的药物,药融云数据库显示目前仅有5项研究针对此靶点展开,并且均处于药物发现阶段。
来特莫韦
来特莫韦是一种非核苷CMV抑制剂(3,4-二氢喹唑啉)。公开资料显示,该产品通过抑制巨细胞病毒末端酶复合物的活性,阻止病毒DNA的加工和包装,从而发挥抗病毒的作用。与DNA聚合酶抑制剂的不同之处在于,来特莫韦对CMV选择性更高,作用强度也有明显提高。
罗普司亭
普司亭(romiplostim)是一种重组蛋白,属于TPO受体激动剂,通过与TPO受体结合可刺激细胞内转录途径,导致血小板生成增加。该药物通过重组DNA技术在大肠杆菌中生产,能模拟人体天然的血小板生成素效果,从而提高血小板计数。当与TPO受体发生结合时,它会促进骨髓巨核细胞集落形成细胞(CFU-Meg)的生长,并通过JAK2和STAT5激酶途径导致血小板生成增加。罗普司亭通过刺激血小板生成素受体来刺激血小板生成的作用机制,与通常使用的通过抑制血小板破坏来提高血小板计数的药物有极大不同。
奥木替韦单抗
奥木替韦单抗注射液是我过自主研发的重组人源抗狂犬病毒单抗,含高效价的抗狂犬病毒单克隆抗体NM57 (IgG1亚型),能特异地中和狂犬病毒糖蛋白保守抗原位点I中的线性中和抗原表位,从而阻止狂犬病毒侵染组织细胞,发挥预防狂犬病的作用。
罗特西普
罗特西普是一种人工合成的ActRIIB-Fc融合蛋白,是美国食药监局(FDA)批准的唯一一个红细胞成熟剂,是FDA批准的首个用于β-地中海贫血的药物。也是10多年来我国首个获批治疗β-地中海贫血的创新药物。
艾伏尼布
艾伏尼布片是一种靶向IDH1突变的口服小分子抑制剂,通过与突变IDH1可逆性结合,降低a-羟戊二酸水平,促进细胞正常分化,从而发挥抗肿瘤效应。艾伏尼布片于2021年8月获FDA批准,是首个且唯一获得美国FDA批准用于IDH1突变胆管癌患者靶向治疗的药物。
钇[90Y]树脂微球
SIR-Spheres®钇[90Y]树脂微球由远大医药集团(00512.HK)联营公司Sirtex公司研发生产并面向全球进行商业化,由放射性核素90Y和微球载体两部分组成,是一款针对肝脏恶性肿瘤的靶向内放射核素产品。其通过介入技术,将SIR-Spheres®钇[90Y]树脂微球注入肝脏肿瘤血管,从而释放高能量β放射线杀灭肿瘤细胞。SIR-Spheres®钇[90Y]微球注射液也是美国食品和药品监督管理局(FDA)正式批准的唯一一款针对结直肠癌肝转移的放射性微球产品,已在全球超过50个国家和地区累计治疗超过12万人次。
奈玛特韦片/利托那韦片组合(Paxlovid )
辉瑞的新冠口服药Paxlovid是今年的明星产品,它包含两种成分,奈玛特韦可以阻断 SARS-CoV-2-3CL 蛋白酶的活性,抑制病毒的转录,利托那韦则减轻细胞色素酶系对奈玛特韦的代谢。今年2月强势登录国内市场,可谓声势浩大,资本也对Paxlovid寄予厚望,此前辉瑞预计今年新冠口服药的销售额能达到220亿美元。但全球来看,销售额远不如预期,最近更是爆出对于肝脏有一定的损伤,这也让这个明星产品蒙上了一层阴影。
乌帕替尼
乌帕替尼是艾伯维公司的一款JAK1选择性抑制剂(upadacitinib,Rinvoq),2019年获美国FDA批准用于对甲氨蝶呤应答不足或不耐受(MTX-IR)的中度至重度活动性类风湿性关节炎(RA)成人患者的治疗。2022年2月24日于中国获批上市,获批适应症为特异性皮炎,就此成为中国第一个治疗特应性皮炎的选择性JAK1抑制剂。首战告捷之后乌帕替尼又连续获批两种适应症,3月25日获批用于重度活动性类风湿关节炎,4月6号获批用于银屑病关节炎,亦是此领域国内首家获批。
重组新型冠状病毒蛋白疫苗(CHO细胞)
安徽智飞龙科马此次获批的疫苗是是首个获批的国产重组新冠病毒蛋白疫苗,此前科兴和北京生物的新冠疫苗均为灭活疫苗。重组蛋白疫苗的特点是成分简单,只选取了病毒上最关键的一部分蛋白,成分清晰简单,相对潜在的安全性安全系数高。
3月1日,智飞龙科马发布了重组新冠蛋白疫苗的三期临床数据。数据显示,在三剂接种7天后,疫苗对18周岁及以上人群(总人群)预防任何严重程度的COVID-19的保护效力为81.43%(95%可信区间为73.35%-87.38%);其中对于COVID-19重症及以上病例的保护效力为92.87%。对变异毒株分析结果显示,三剂接种7天后对Delta变异株的保护效力为81.38%。
依帕伐单抗
依帕伐单抗Gamifant(Emapalumab-lzsg)是一种干扰素γ(INFγ)阻断抗体,是第一个也是目前唯一一个获批治疗原发性噬血细胞性淋巴组织细胞增多症(HLH)的药物。最初由Novimmune SA公司开发,Swedish Orphan Biovitrum AB于2018年通过独家许可协议获得了依帕伐单抗的全球权益。
Inebilizumab
Inebilizumab是国内首款获批的CD19单抗,用于治疗罕见疾病神经脊髓炎谱系障碍。国内市场,它的竞争对手为CD19/CD3双特异性抗体倍林妥莫双抗,此药于2020年12月获批进口。
参考来源:
[1] NMPA官网
[2] 药融云
[3]药物相关文献
(转自sigima 药通社)